Tìm hiểu về khí NH3-Amoniac
Amoniac (NH3) là một hợp chất vô cơ quan trọng, được sử dụng rộng rãi trong nhiều ngành công nghiệp và đời sống. Với cấu trúc phân tử đặc trưng và tính chất độc đáo, amoniac đóng vai trò thiết yếu trong sản xuất phân bón, hóa chất, dược phẩm và nhiều ứng dụng khác. Bài viết này sẽ cung cấp cho bạn một cái nhìn toàn diện về amoniac, bao gồm định nghĩa, cấu trúc, tính chất, nguồn gốc, ảnh hưởng đến sức khỏe và môi trường, cũng như các ứng dụng quan trọng của nó.
1.Khái Quát về Amoniac (NH3): Định Nghĩa, Cấu Trúc và Tính Chất
Định Nghĩa Amoniac (NH3)
Amoniac (NH3) là một hợp chất vô cơ, được cấu tạo bởi một nguyên tử nitơ (N) và ba nguyên tử hiđro (H). Nó là một chất khí không màu, có mùi khai nồng nặc và rất dễ hòa tan trong nước. Amoniac là một hóa chất quan trọng, được ứng dụng rộng rãi trong nhiều ngành công nghiệp và đời sống.
Cấu Trúc Phân Tử Amoniac (NH3)
Amoniac có cấu trúc hình chóp tam giác, với nguyên tử nitơ ở đỉnh chóp và ba nguyên tử hiđro ở đáy bằng, liên kết với nhau bằng các liên kết cộng hóa trị. Góc liên kết N-H-H là khoảng 107 độ, nhỏ hơn 109,5 độ do cặp electron tự do trên nguyên tử nitơ đẩy các cặp electron liên kết.
Thành Phần Hóa Học của Amoniac (NH3)
Mỗi phân tử amoniac chứa một nguyên tử nitơ và ba nguyên tử hiđro. Khối lượng phân tử của amoniac là 17,03 g/mol.
Tính Chất Vật Lý của Amoniac (NH3)
- Trạng thái: Khí không màu, có mùi khai nồng nặc
- Khối lượng riêng: 0,771 g/L (ở 0 độ C và áp suất 1 atm)
- Điểm nóng chảy: -77,73 độ C
- Điểm sôi: -33,34 độ C
- Độ hòa tan: Hòa tan tốt trong nước, tạo dung dịch kiềm yếu
- Tính độc: Amoniac là chất độc, gây kích ứng đường hô hấp, mắt và da
Tính Chất Hóa Học của Amoniac (NH3)
- Tính bazơ yếu: Amoniac tác dụng với nước tạo thành dung dịch amoni hydroxit (NH4OH). Dung dịch này có tính bazơ yếu, làm quỳ tím hóa xanh.
- Tính khử: Amoniac là chất khử mạnh, dễ bị oxi hóa. Ví dụ, nó cháy trong không khí tạo thành nitơ và hơi nước.
2.Cấu Tạo và Thành Phần của Amoniac (NH3)
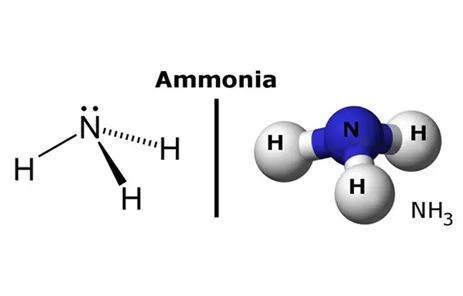
Cấu Trúc Phân Tử Amoniac (NH3)
Amoniac có cấu trúc phân tử hình chóp tam giác, với nguyên tử nitơ ở đỉnh chóp và ba nguyên tử hiđro ở đáy bằng, liên kết với nhau bằng các liên kết cộng hóa trị. Góc liên kết N-H-H là khoảng 107 độ, nhỏ hơn 109,5 độ do cặp electron tự do trên nguyên tử nitơ đẩy các cặp electron liên kết.
| Thành Phần | Số Lượng |
| Nguyên tử nitơ (N) | 1 |
| Nguyên tử hiđro (H) | 3 |
| Khối lượng phân tử | 17,03 g/mol |
Cấu Hình Electron của Amoniac (NH3)
Cấu hình electron của amoniac (NH3) như sau:
- Nguyên tử nitơ (N): 1s^2 2s^2 2p^3
- Các electron liên kết: 3 cặp electron liên kết N-H
- Electron tự do: 1 cặp electron tự do trên nguyên tử nitơ
Sự tồn tại của cặp electron tự do trên nguyên tử nitơ làm cho góc liên kết N-H-H nhỏ hơn 109,5 độ, góp phần tạo nên cấu trúc chóp tam giác đặc trưng của amoniac.
Thành Phần Hóa Học của Amoniac (NH3)
Mỗi phân tử amoniac (NH3) bao gồm:
- 1 nguyên tử nitơ (N)
- 3 nguyên tử hiđro (H)
Tỷ lệ các nguyên tố trong amoniac là:
- Nitơ (N): 14,01 g/mol
- Hiđro (H): 3 × 1,01 g/mol = 3,03 g/mol
- Khối lượng phân tử: 14,01 g/mol + 3,03 g/mol = 17,03 g/mol
3.Đặc Tính Vật Lý và Hóa Học của Amoniac (NH3)
Tính Chất Vật Lý của Amoniac (NH3)
Trạng thái và Mùi:
- Amoniac là một chất khí không màu, có mùi khai nồng nặc.
Khối Lượng Riêng:
- Khối lượng riêng của amoniac là 0,771 g/L (ở 0 độ C và áp suất 1 atm).
Nhiệt Độ Nóng Chảy và Sôi:
- Điểm nóng chảy của amoniac là -77,73 độ C.
- Điểm sôi của amoniac là -33,34 độ C.
Độ Hòa Tan:
- Amoniac hòa tan tốt trong nước, tạo thành dung dịch kiềm yếu.
Tính Độc:
- Amoniac là chất độc, gây kích ứng đường hô hấp, mắt và da.
Tính Chất Hóa Học của Amoniac (NH3)
Tính Bazơ Yếu:
- Amoniac tác dụng với nước tạo thành dung dịch amoni hydroxit (NH4OH), có tính bazơ yếu.
- Dung dịch NH4OH làm quỳ tím hóa xanh.
Tính Khử:
- Amoniac là chất khử mạnh, dễ bị oxi hóa.
- Khi cháy trong không khí, amoniac sẽ tạo thành nitơ và hơi nước.
4.Nguồn Gốc và Quá Trình Tạo Thành Amoniac (NH3)
Nguồn Gốc Tự Nhiên của Amoniac (NH3)
- Amoniac được tạo ra trong tự nhiên thông qua các quá trình sinh học và địa hóa.
- Trong đó, quá trình phân hủy protein và vi khuẩn nitrosomas là nguồn gốc chính của amoniac trong tự nhiên.
Quá Trình Tạo Thành Amoniac Nhân Tạo
- Công nghiệp sản xuất amoniac chủ yếu dựa trên quá trình Haber-Bosch, trong đó nitơ và hiđro được phản ứng với nhau ở nhiệt độ và áp suất cao.
- Hiện nay, hầu hết amoniac được sản xuất thông qua quá trình Haber-Bosch với sự trợ giúp của các xúc tác như sắt oxy hóa.
5.Ảnh Hưởng của Amoniac (NH3) đến Sức Khỏe Con Người
Tác Động Độc Hại của Amoniac
- Amoniac là chất độc, gây kích ứng mạnh đối với đường hô hấp, mắt và da khi tiếp xúc.
- Hít phải amoniac có thể gây ra các triệu chứng như ho, khó thở, đau họng, giảm khả năng nhìn và các vấn đề về da.
- Tiếp xúc với nồng độ cao có thể dẫn đến tổn thương phổi, thậm chí tử vong.
Biện Pháp Phòng Ngừa và Sơ Cứu
- Cần tránh tiếp xúc trực tiếp với amoniac, đặc biệt ở nồng độ cao.
- Khi bị phơi nhiễm, cần rửa sạch bằng nước sạch và đưa nạn nhân đến cơ sở y tế ngay lập tức.
- Sử dụng các trang thiết bị bảo hộ cá nhân như mặt nạ phòng độc khi tiếp xúc amoniac.
6.Tác Động của Amoniac (NH3) đến Môi Trường
Ô Nhiễm Không Khí do Amoniac
- Amoniac là một chất khí độc hại, khi thoát ra môi trường có thể gây ô nhiễm không khí cục bộ.
- Nồng độ amoniac cao trong không khí có thể gây hại cho người và động vật.
Ảnh Hưởng đến Hệ Sinh Thái Thủy Vực
- Amoniac có thể bị rửa trôi vào nguồn nước, gây ô nhiễm nước và ảnh hưởng xấu đến các hệ sinh thái thủy vực.
- Sự có mặt của amoniac có thể làm tăng độ pH, thay đổi thành phần các loài và ảnh hưởng đến cân bằng sinh học.
Biện Pháp Hạn Chế Ô Nhiễm do Amoniac
- Cần có các quy định, tiêu chuẩn về mức độ amoniac cho phép trong không khí và nguồn nước.
- Áp dụng công nghệ xử lý khí thải và nước thải hiệu quả để giảm thiểu lượng amoniac thoát ra môi trường.
- Nâng cao ý thức bảo vệ môi trường và sử dụng amoniac an toàn trong sản xuất, vận chuyển và sử dụng.
7.Ứng Dụng của Amoniac (NH3) trong Đời Sống và Sản Xuất
Sử Dụng Amoniac trong Nông Nghiệp
- Amoniac là thành phần quan trọng trong sản xuất phân bón nitrogen, phục vụ nhu cầu sản xuất nông nghiệp.
- Các dạng phân bón chứa amoniac như urê, amoni sulfat, amoni nitrat được sử dụng rộng rãi để bón cho cây trồng.
Ứng Dụng Amoniac trong Công Nghiệp Hóa Chất
- Amoniac là nguyên liệu quan trọng để sản xuất nhiều hóa chất khác như axít nitric, amoni nitrat, amoni sulfat.
- Các hóa chất này được sử dụng rộng rãi trong sản xuất phân bón, thuốc nổ, chất tẩy rửa, v.v.
Vai Trò của Amoniac trong Công Nghiệp Dược Phẩm
- Amoniac được sử dụng làm nguyên liệu trong sản xuất một số loại thuốc và dược phẩm.
- Ví dụ, amoniac được dùng để sản xuất sulfanilamid, một loại thuốc kháng sinh.
Ứng Dụng Amoniac trong Lĩnh Vực Công Nghiệp Khác
- Amoniac được sử dụng làm chất làm lạnh, chất tẩy rửa, chất ức chế ăn mòn, v.v.
- Ngoài ra, amoniac còn được dùng trong các quá trình hàn, gia công kim loại và sản xuất nhiên liệu.
8.Các Ứng Dụng Quan Trọng của Amoniac (NH3) trong Công Nghiệp Hóa Chất
Sản Xuất Phân Bón Nitơ
- Amoniac là nguyên liệu chính để sản xuất các loại phân bón nitơ như urê, amoni sulfat, amoni nitrat.
- Các loại phân bón này đóng vai trò quan trọng trong nông nghiệp để cung cấp dưỡng chất cho cây trồng và tăng năng suất.
Sản Xuất Hóa Chất
- Amoniac được sử dụng làm nguyên liệu để sản xuất nhiều hóa chất khác như axít nitric, amoni nitrat, amoni sulfat.
- Các hóa chất này có ứng dụng rộng rãi trong công nghiệp hóa chất, từ sản xuất phân bón đến thuốc nổ.
Sản Xuất Thuốc Kháng Sinh
- Trên thị trường, amoniac được sử dụng làm nguyên liệu để sản xuất một số loại thuốc kháng sinh như sulfanilamid.
- Các loại thuốc này đóng vai trò quan trọng trong điều trị các bệnh nhiễm khuẩn.
Sản Xuất Chất Tẩy Rửa
- Amoniac cũng được sử dụng trong sản xuất chất tẩy rửa do tính bazơ của nó giúp phản ứng với các chất ô nhiễm.
- Chất tẩy rửa chứa amoniac thường được sử dụng để làm sạch bề mặt trong gia đình và công nghiệp.
Sản Xuất Chất Làm Lạnh
- Trên thị trường, amoniac được sử dụng làm chất làm lạnh trong hệ thống điều hòa không khí và máy lạnh.
- Tính khử mạnh của amoniac giúp nó hấp thụ nhiệt hiệu quả, làm mát không gian một cách hiệu quả.
4.Nhà cung cấp khí chất lượng uy tín
Công ty Cổ phần khí chuẩn Toàn cầu là nhà sản xuất và phân phối tất cả các loại khí hàng đầu tại Việt Nam.
Quý khách hàng nếu có nhu cầu sử dụng khí chuẩn, hãy liên hệ với chúng tôi qua hotline: 0858.446.446; 0814144144 hoặc truy cập wedsite: khichuanvietnam.com để được tư vấn.



